19/07/2024
El estudio, liderado por el Servicio de Hematología del Hospital de Salamanca y publicado en la revista de alto impacto ‘British Journal of Haematology’, demuestra la utilidad de la secuenciación masiva que, a partir de una simple muestra de sangre, puede detectar la presencia de ADN circulante tumoral tanto en el momento del diagnóstico como durante el seguimiento
Esta estrategia, mínimamente invasiva y accesible en cualquier momento durante el curso de la enfermedad, ha demostrado su efectividad en el 90% de las muestras analizadas y permite avanzar en la medicina personalizada de precisión
Investigadores del Instituto de Investigación Biomédica de Salamanca (IBSAL) —Consejería de Sanidad de la Junta de Castilla y León, Universidad de Salamanca (USAL) y Consejo Superior de Investigaciones Científicas (CSIC) — validan una pionera herramienta de secuenciación masiva para un mejor abordaje de los pacientes con linfoma a través de la biopsia líquida, tanto en el momento del diagnóstico como durante su seguimiento, para avanzar en la medicina personalizada de precisión. La biopsia líquida es una nueva metodología que permite detectar en una simple muestra fragmentos del ADN del tumor liberado a la sangre del paciente (ADN circulante tumoral).
En un estudio publicado en la revista de alto impacto British Journal of Haematology y liderado por el Servicio de Hematología del Complejo Asistencial Universitario de Salamanca (CAUSA), se ha demostrado que abordar el estudio del tumor de esta forma mínimamente invasiva, con la recogida de una muestra de sangre periférica, permite determinar la presencia de ADN circulante tumoral (ADNct) para su caracterización molecular y la evaluación temprana de la enfermedad mínima residual (persistencia de la enfermedad después del tratamiento), lo que se traduce en una mejor estratificación de los pacientes en distintos grupos de riesgo, que podrían beneficiarse en un futuro próximo de un tratamiento más preciso.
Como explica la Dra. María Eugenia Sarasquete, investigadora de la Unidad de Biología Molecular del Servicio de Hematología del CAUSA junto a su compañero el Dr. Miguel Alcoceba, firmantes principales del artículo, los resultados de la investigación demuestran que “con un simple pinchazo” que requiere la biopsia líquida “hemos podido detectar un marcador tumoral en el 90% de las muestras”, lo cual “es realmente efectivo en el momento del diagnóstico para conocer el tipo de tumor y sus alteraciones moleculares”. Pero, además, “una vez identificados los marcadores específicos del tumor, podemos realizar su seguimiento y determinar así si la cantidad de ADN circulante tumoral se ha reducido o ha desaparecido con el tratamiento, lo que conllevaría un mejor pronóstico”.

Para llevar a cabo este proceso, se ha utilizado una herramienta desarrollada dentro del grupo colaborativo europeo EuroClonality, formado por más de veinte laboratorios del área de onco-hematología, que ha diseñado un panel de secuenciación masiva exclusivo para el estudio de leucemias y linfomas (Euroclonality-NDC). Se trata de un panel de alta sensibilidad que se había probado con éxito en muestras de tumor obtenidas por biopsia clásica y que ahora se ha validado en biopsia líquida en el Servicio de Hematología de Salamanca en colaboración con The Patrick G Johnston Centre for Cancer Research, de la Universidad Queens de Belfast (Reino Unido).
Además de su efectividad, la estrategia resulta poco costosa para el Sistema Nacional de Salud, es menos invasiva y molesta para el paciente, y “tiene una ventaja fundamental, porque ofrece información global del tumor —en una biopsia clásica se obtiene solo una muestra de una región concreta del tumor en un momento determinado- y, además, los estudios se pueden llevar a cabo con una mayor frecuencia —solo es necesario una muestra de sangre — lo que nos permite un seguimiento más estrecho de los pacientes y poder detectar la enfermedad antes de su recaída clínica”, como explica la investigadora.
Aplicable a todo tipo de linfomas
El linfoma es un tipo de cáncer hematológico que provoca un crecimiento anormal y descontrolado de los linfocitos, un tipo de glóbulos blancos que se producen en la médula ósea y se encargan de proteger nuestro organismo. La incidencia es de 12 casos por 100.000 habitantes y año, lo que supone unos 3000 nuevos diagnósticos en España cada año. Dentro del linfoma no Hodgkin, el difuso de células B grandes es el subtipo más común y supone un 30% de los casos. Es agresivo y biológicamente muy heterogéneo, por lo que resulta esencial identificar parámetros clínicos y biomarcadores que puedan ayudar a mejorar su abordaje. Este tipo de linfoma se localiza habitualmente en los ganglios linfáticos, donde las células tumorales permanecen “escondidas”, por lo que las exploraciones utilizadas para analizarlos son más parecidas a las que se usan en los estudios de los tumores sólidos que en los de las leucemias. Por eso, la biopsia líquida a partir de una muestra de sangre se postula como una herramienta muy útil y mínimamente invasiva para su estudio.
En la actualidad, la tomografía por emisión de positrones (PET) combinada con la tomografía computarizada (PET/TC) se considera el estándar para la evaluación de la respuesta al tratamiento y el seguimiento de los pacientes, pero son técnicas de imagen costosas, que conllevan la sobre-exposición del afectado a la radiación y además presentan en algunos casos falsos positivos/negativos que podrían llevar a una toma de decisiones inapropiada.
En este contexto, el objetivo de los investigadores del IBSAL fue buscar “una herramienta más sensible, más específica y menos invasiva para monitorizar en tiempo real la respuesta terapéutica de los pacientes” con la que poder anticiparse en la toma de decisiones y personalizar el tratamiento según las necesidades de cada afectado.
El estudio incluyó una serie prospectiva de 68 pacientes con linfoma difuso de células B grandes desde abril de 2017 hasta mayo de 2020, diagnosticados en el Hospital de Salamanca, y también en el Hospital Clínico de Valladolid y los Complejos Asistenciales de León y Burgos, con el objetivo de investigar la utilidad de la biopsia líquida utilizando un enfoque de secuenciación masiva (EuroClonality-NDC) que permitiera analizar el valor clínico y pronóstico del ADN circulante tumoral.
Con los prometedores resultados obtenidos, y una vez que el Servicio de Hematología cuenta ya con esta herramienta —durante el estudio las muestras tuvieron que ser enviadas al laboratorio de Belfast—“el próximo objetivo será implementar esta estrategia de forma rutinaria, ya que, además, es aplicable a cualquier tipo de linfoma”, como comentan los investigadores. Pero además, en previsión de lograr esta importante mejora para el manejo de estos pacientes y dado el más que probable aumento en el número de muestras, el Servicio de Hematología ha adquirido también un robot para lograr un procesamiento de forma automática, reproducible y mucho más rápido y poder así dar una respuesta en tiempo real en un corto plazo.
Modelo útil y homogéneo a nivel nacional
Para que esta estrategia de biopsia líquida se incorpore a la práctica clínica rutinaria, se precisa aun un trabajo considerable de estandarización de las técnicas, así como su validación en series más amplias de pacientes. Por ello, el Hospital de Salamanca, avalado también por esta publicación científica de alto impacto, mantiene conversaciones con otros centros hospitalarios españoles dentro del Grupo Español de Linfomas (GELTAMO) para avanzar en la implementación a nivel nacional de esta estrategia pionera basada en biopsia líquida en el abordaje de los linfomas, y que “seamos capaces de trabajar de forma conjunta para que todos los pacientes reciban la misma atención en cualquier centro y esto se traduzca en definitiva en un seguimiento más personalizado y una mejora en la calidad de vida” , tal y como concluyen los doctores María Eugenia Sarasquete y Miguel Alcoceba.
Este estudio colaborativo internacional ha sido coordinado desde el Servicio de Hematología de Salamanca y los grupos del IBSAL, CANC-05, Biología molecular y celular de hemopatías (dirigido hasta hace poco tiempo por el Dr. Ramón García-Sanz y actualmente por la Dra. Norma Gutiérrez), y CANC-28, neoplasias linfoproliferativas maduras (dirigido por el Dr. Alejandro Martín García-Sancho). Además, han participado facultativos de los Servicios de Anatomía Patología, Medicina Nuclear y Radiofísica y Protección Radiológica, y hematólogos de los hospitales de Burgos, León y Clínico de Valladolid, además del Patrick G Johnston Centre for Cancer Research de Belfast (Reino Unido) y el Grupo de trabajo cooperativo de linfomas y procesos linfoproliferativos de la Asociación Castellano-Leonesa de Hematología y Hemoterapia.
Por último, los autores quieren agradecer a los pacientes por su participación en este tipo de estudios en los que donan sus muestras con fines de investigación, ya que, sin su colaboración altruista, trabajos como este no verían la luz.
El IBSAL
El Instituto de Investigación Biomédica de Salamanca (IBSAL) se constituyó el 21 de marzo de 2011 mediante un convenio firmado por la Consejería de Sanidad de la Junta de Castilla y León y la Universidad de Salamanca, al que se sumó en febrero de 2012 el Consejo Superior de Investigaciones Científicas (CSIC). En él se integra y coordina la investigación biosanitaria que se lleva a cabo en el Hospital Universitario de Salamanca, la Gerencia de Atención Primaria de Salamanca y el área biosanitaria de la Universidad de Salamanca, incluyendo el Instituto de Neurociencias de Castilla y León y el Instituto de Biología Molecular y Celular del Cáncer.
Su actividad científica se estructura en seis áreas, con un total de 84 grupos de investigación: Cáncer (23 grupos); Cardiovascular, Renal y Respiratorio (11); Neurociencias (12); Enfermedades Infecciosas, Inflamatorias y Metabólicas (17); Terapia Génica y Celular y Trasplantes (6) y Atención Primaria, Salud Pública y Farmacología (15).
Artículo de referencia:
Alcoceba M, Stewart JP, García-Álvarez M, Díaz LG, Jiménez C, Medina A, et al. Liquid biopsy for molecular characterization of diffuse large B-cell lymphoma and early assessment of minimal residual disease. Br J Haematol. 2024;00:1–13. undefined
Pie de foto 1: Los doctores Alejandro Martín, María Eugenia Sarasquete, Norma C Gutiérrez y Miguel Alcoceba, participantes en el estudio.
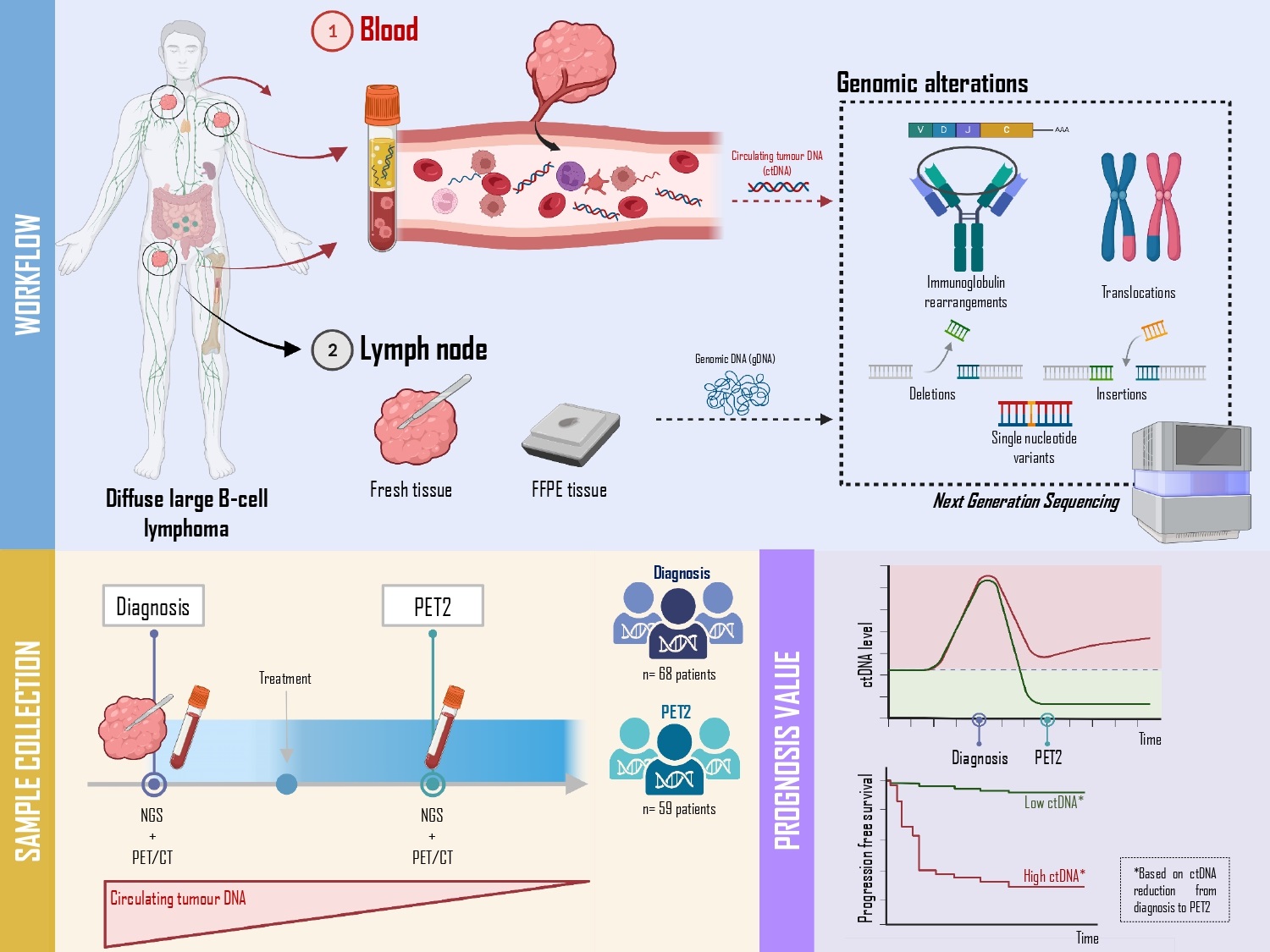
Pie de foto 2: Flujo de trabajo. La parte superior representa el estudio en paralelo de biopsia líquida en sangre periférica (1) frente a la biopsia tradicional de un ganglio (2). En ambos casos el objetivo final es identificar las alteraciones genéticas del tumor (traslocaciones y mutaciones) mediante técnicas de secuenciación masiva (Next Generation Sequencing). La parte inferior refleja como la carga tumoral (ADN circulante tumoral, ADNct) disminuye una vez los pacientes reciben el tratamiento, y como aquellos que reducen o incluso negativizan el nivel de ADNct (verde) tiene un mejor pronóstico que aquellos que no lo reducen (rojo).
Más información y contacto:
Esta dirección de correo electrónico está siendo protegida contra los robots de spam. Necesita tener JavaScript habilitado para poder verlo.