Investigadores del Instituto de Investigación Biomédica de Salamanca y del Centro de Investigación del Cáncer (CSIC-Universidad de Salamanca-FICUS) han demostrado que la proteína C3G suprime el crecimiento tumoral en el linfoma de células B, pero también que favorece la metástasis.
El hallazgo ha sido publicado en la revista Cell Communication and Signaling, ha sido codirigido por Carmen Guerrero y José María De Pereda, y se ha basado en experimentos con modelos celulares y animales.
A partir de estos resultados Carmen Guerrero resalta que «C3G podría predecir si el linfoma se extenderá y ser un objetivo para nuevos tratamientos que frenen el tumor sin favorecer las metástasis”.
Mediante esta investigación se ha descubierto que la proteína C3G (RapGEF1) desempeña un papel dual en el linfoma de células B, un tipo de cáncer hematológico. Mientras su hiperactivación limita la proliferación de las células tumorales, al mismo tiempo aumenta su capacidad migratoria y metastásica.
La proteína C3G es como un «interruptor» que normalmente activa de forma controlada a Rap1, una molécula esencial para que las células se adhieran entre sí, crezcan o se muevan. En algunos pacientes con linfoma no Hodgkin, una mutación (Y554H) rompe el freno natural de C3G, dejándola siempre encendida. El equipo investigador ha recreado esta mutación (Y564H en ratones) en células de linfoma usando el editor genético CRISPR para entender qué consecuencias tiene.
Resultados principales en modelos celulares
En el experimento, las células mutadas C3G-Y564H tenían Rap1 siempre encendido, tanto en reposo como al estimular el receptor BCR de las células B o la molécula CXCL12. Este exceso de Rap1 bloqueó la orden de crecer sin control al reducir c-Raf, haciendo que las células crecieran hasta un 50 % menos en 72 horas (este porcentaje ha sido medido por citometría y microscopía viva Incucyte). Además, murieron más fácilmente bajo estrés, porque tenían menos Bcl-xL, una proteína que normalmente las protege de la muerte celular (apoptosis). La hiperactivación de Rap1 por la mutación C3G-Y564H redujo esta protección vital.
Al mismo tiempo, la mutación bajó la actividad de Rac2, una proteína que ayuda a las células sanguíneas a ‘pegarse’ bien a su entorno. Las células mutadas se adherían menos a proteínas del entorno celular (fibrinógeno y fibronectina) y a capas de vasos sanguíneos (células HUVEC), pero escapaban más fácilmente –hasta un 50 % más– hacia otros lugares, guiadas por señales químicas. El análisis de genes mostró miles de cambios en mecanismos de movimiento y adhesión.
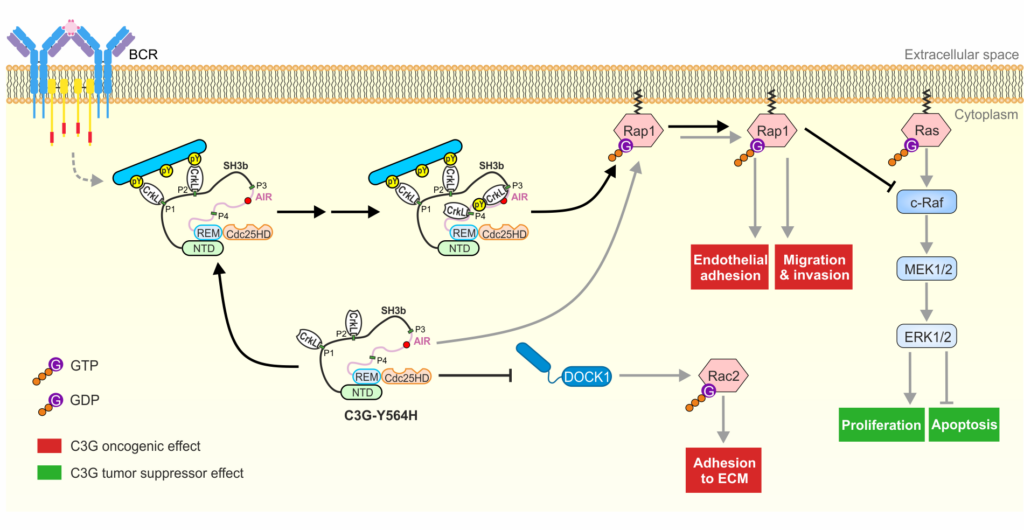
Representación esquemática de las vías moleculares de la proteína C3G.
Validación en modelos animales
Mediante el empleo de modelos animales (ratones) se simula la enfermedad humana y se estudia cómo las células cancerosas se diseminan por el cuerpo en condiciones fisiológicas reales. Por esta razón, el grupo de investigación inyectó células A20 a ratones BALB/c inmunocompetentes. Tras 21 días, los análisis revelaron que los ratones con células C3G-Y564H desarrollaron más focos metastásicos en hígado –pequeños, pero más numerosos– que los controles. Este experimento confirmó la mayor capacidad invasiva de las células mutadas C3G-Y564H. Los clones con menor expresión de C3G mostraron aún mayor diseminación y validan el doble rol de esta proteína.
Alba Morán-Vaquero (primera firmante de la publicación) resalta: “Estos resultados en modelos in vivo validan el doble efecto de C3G: supresor del crecimiento primario a través de Rap1, pero promotor de metástasis por inhibición de Rac2 y menor adhesión celular”.
Financiación y colaboración institucional
El estudio forma parte de la Grupos Estratégicos de la Junta de Castilla y León y cuenta con financiación del Ministerio de Ciencia, Innovación y Universidades, ISCIII, Fundación Científica AECC y fondos FEDER. Participan investigadores del Investigación Biomédica de Salamanca (IBSAL), el Centro de Investigación del Cáncer (CSIC-USAL- FICUS) y la Universidad de Leiden (Países Bajos).